臨床前研究
新藥研發(fā)風險大,成功率低,據統(tǒng)計,每合成或分離10,000個化合物,平均只有1個化合物能夠真正上市。為申請藥品注冊而進行的臨床前研究,包括藥物的合成工藝、提取方法、理化性質及純度、劑型選擇、處方篩選、制備工藝、檢驗方法、穩(wěn)定性、藥理、毒理、動物藥代動力學等研究。
臨床前研究階段的終極目標是確定首次人體研究的合適給藥劑量,并選擇合適的臨床給藥制劑。近年來,FDA等法規(guī)機構都在倡導使用模型引導的藥物研發(fā)MiDD加速新藥或仿制藥研發(fā)進程。
我們提供了系列模型引導的藥物研發(fā)MiDD工具,提高臨床前研究的成功率。
凡默谷臨床前研究解決方案

預測口服吸收,探討限制吸收和生物利用度的關鍵因素
根據藥物理化與生物藥劑學性質,對藥物體內ADME過程進行預測,分析化合物或處方因素(如粒徑、溶解度、增溶、沉淀等)對藥物體內吸收或PK的影響,找到關鍵影響因素,為化合物優(yōu)化或制劑處方開發(fā)提供指導;也為毒理試驗給藥劑量提供指導。
預測動物PK曲線及ADME過程研究
利用藥物體外理化參數、體外代謝試驗數據或者體內PK數據,建立不同動物的PBPK模型,深入研究動物體內的ADME過程,分析潛在的作用機制;考察劑量、劑型變化后的PK改變;為動物毒理學研究提供相關支持等。
種屬外推,預測首次人體PK
結合藥物的體外ADME性質參數及動物體內PK數據,建立、驗證、優(yōu)化不同種屬的PBPK模型,并進一步預測人體PK曲線及PK參數,探討人體的暴露特征:指導化合物的優(yōu)化與篩選,為I期臨床試驗設計和給藥劑量提供指導,并對藥物體內ADME過程提供機理解釋,為申報資料的科學性提供依據。
考察食物效應
評估受試者在不同食物狀態(tài)下(空腹、標準餐、高脂高熱餐等)給藥后體內的PK曲線變化,以此指導制劑處方的調整(尋找避免食物效應的關鍵因素),以及餐前餐后臨床PK試驗的臨床方案設計等。
初步考察藥物相互作用DDI風險
根據DDI體外試驗數據,初步考察代謝酶或轉運體介導的DDI風險,為臨床給藥方案設計、臨床DDI試驗開展提供指導。
安全性評估和毒理學研究
通過毒性預測軟件(ADMET Predictor)可預測化合物的多種毒性,從而系統(tǒng)地評估化合物潛在的安全性風險,并可以免除部分法規(guī)要求的毒性測試。通過PBPK建模平臺可以在早期階段就確定最大耐受劑量。此外,通過DILIsym?平臺與體外數據的整合,可以了解化合物存在哪些肝臟毒性,從而幫助化合物下一步開發(fā)的優(yōu)先順序。
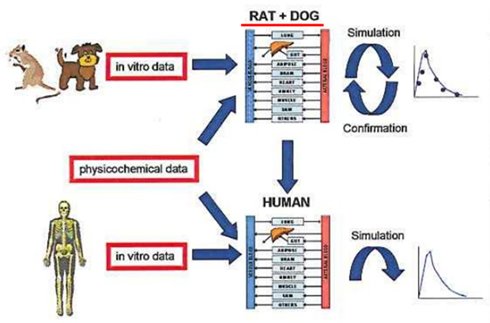
采用PBPK進行在種屬間外推的流程圖
點擊查看其它解決方案


